Капли датского короля
Капли датского короля.
Российская военная фармакопея, 1913 год.


Наше предприятие осуществляет заготовку, сушку и реализацию пряно-ароматического и лекарственного…
Государственная Фармакопея (ГФ РБ) Том 2 стр. 457-459. Эхинацеи пурпурной трава.
ЭХИНАЦЕИ ПУРПУРНОЙ ТРАВА
Echinaceae purpureae herba
PURPLE CONEFLOWER HERB
ОПРЕДЕЛЕНИЕ
Собранная в фазу цветения, цельная или резаная и высушенная трава многолетнего травянистого растения Echinacea purpurea (L.) Moench. Содержит не менее 0,1 % суммы кафтаровой кислоты (С13Н12О9; М.м. 312,2) и цикориевой кислоты (С22Н18О12; М.м. 474,3) в пересчете на сухое сырье или не менее 2,1 % суммы производных оксикоричных кислот в пересчете на цикориевую кислоту (С22Н18О12; М.м. 474,3) в сухом сырье.
ПОДЛИННОСТЬ (ИДЕНТИФИКАЦИЯ)
А. Внешние признаки (#2.8.3). Куски стеблей, листьев, цельные и частично разрушенные цветочные корзинки, цветки, бутоны, реже незрелые плоды. Стебли цилиндрические, ребристые, голые или (редко) жесткоопущенные, диаметром до 1 см. Листья черешковые, продолговато-яйцевидные, яйцевидно-ланцетные или ланцетные, остроконечные, неравнокрупнозубчатые, реже цельнокрайние, с 3—5 продольными жилками, жесткие, шероховатые от короткощетинистого опушения. Цветочные корзинки с выпуклым, полым, густоусаженным прицветниками цветоложем. Обертка блюдцевидная, трехрядная; листочки обертки черепитчаторасположенные, ланцетные, остроконечные, отогнутые, опущенные с внешней стороны, голые по краям. Прицветники узколанцетные, с шиловидным окончанием, превышающие по длине трубчатые цветки. Краевые цветки язычковые, длиной до 6 см, пестичные, бесплодные, с двух-трехзубчатым отгибом, снаружи опушенным. Срединные цветки трубчатые, обоеполые, с пятизубчатым венчиком. Плоды — семянки обратнопирамидальные, четырехгранные, к основанию суженные, с хохолком в виде короны с неравномерными зубчиками. Цвет стеблей зеленый, желтовато-зеленый, иногда с розовато-красными или фиолетово-красными пятнами; листьев — зеленый; листочков обертки — серовато-зеленый или зеленый; цветков — розовато-красный или фиолетово-красный; плодов — зеленый или зеленовато-коричневый. Запах слабый.
В. Микроскопия (#2.8.3). При просматривании листа с поверхности видны клетки эпидермиса с извилистыми стенками. Устьица овальные, окружены 2—6 околоустьичными клетками (аномоцитный тип); расположены на обеих сторонах листа, на нижней их больше. Над жилками клетки эпидермиса имеют прямые стенки и вытянуты вдоль них. По жилкам и по краю листа встречаются простые длинные одноклеточные волоски и простые 2—4-клеточные остроконечные волоски со спавшейся конечной клеткой, часто опадающей; простые 1—4-клеточные волоски, иногда с заметным утолщением стенок; изредка встречаются железистые волоски, состоящие из 1—2-клеточной ножки и одноклеточной овальной головки, заполненной желтовато-коричневым содержимым. Клетки у основания волосков расположены радиально и образуют розетку. Клетки эпидермиса язычкового и трубчатого цветков на зубчиках сосочковидные, на остальных частях цветков со слабоизвилистыми стенками, над жилками — с прямыми стенками. Устьица мелкие, овальные, погруженные, окружены 4—6 околоустьичными клетками (аномоцитный тип). Простые 2—3-клеточные волоски с острым концом расположены преимущественно по жилкам. Железки состоят из 10—12 выделительных клеток, расположенных в два ряда.
ЕФ С. Тонкослойная хроматография (2.2.27).
Испытуемый раствор. К 1,0 г измельченного сырья (355) прибавляют 10 мл метанола Р и обрабатывают ультразвуком в течение 5 мин. Центрифугируют и собирают надосадочную жидкость.
Раствор сравнения. 0,5 мг кофейной кислоты Р и 0,5 мг хлорогеновой кислоты Р растворяют в 5,0 мл метанола Р.
Пластинка: ТСХ пластинка со слоем силикагеля Р (5—40 мкм) [или ТСХ пластинка со слоем силикагеля Р (2—10 мкм)].
Подвижная фаза: кислота муравьиная безводная Р — вода Р — метилэтилкетон Р — этилацетат Р (3:3:9:15, об/об/об/об).
Наносимый объем пробы: 25 мкл [5 мкл] испытуемого раствора и 10 мкл [2 мкл] раствора сравнения в виде полос.
Фронт подвижной фазы: не менее 15 см [5 см] от линии старта.
Высушивание: в токе холодного воздуха в течение 10 мин, затем при температуре 100°С в течение 2 мин.
Проявление: горячую пластинку опрыскивают раствором 5 г/л аминоэтилового эфира дифенилборной кислоты Р в этилацетате Р. Через 30 мин пластинку просматривают в ультрафиолетовом свете при длине волны 365 нм.
Результаты: ниже приведена последовательность зон хроматограмм раствора сравнения и испытуемого раствора. На хроматограмме испытуемого раствора могут обнаруживаться другие слабые флуоресцирующие зоны синего цвета.
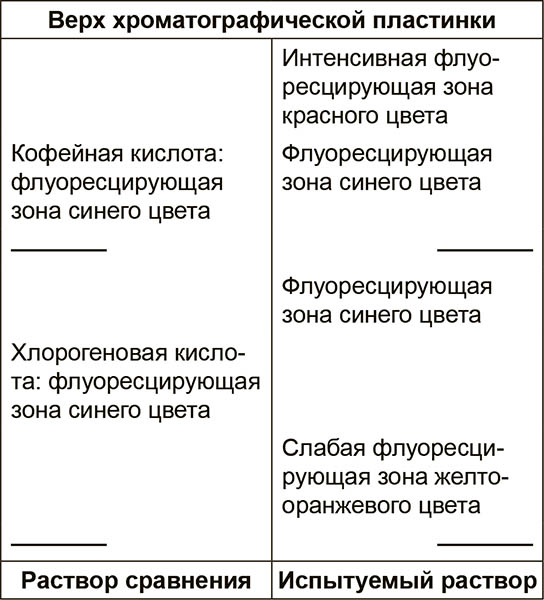
ИСПЫТАНИЯ (ЧИСЛОВЫЕ ПОКАЗАТЕЛИ)
Допустимые примеси (#2.8.2). Несырьевые части растения: стебли — не более 55 %. Органические примеси: не более 2,5 %. Минеральные примеси: не более 1 %.
Потеря в массе при высушивании (2.2.32). Не более 13,0 %. 2,000 г измельченного сырья (2000) сушат при температуре от 100°С до 105°С.
ЕФ: Общая зола (2.4.16). Не более 12,0%.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ЕФ: Определение содержания суммы кафтаровой кислоты и цикориевой кислоты.
Жидкостная хроматография (2.2.29).
Испытуемый раствор. 0,500 г измельченного сырья (355) помещают в мерную колбу вместимостью 100 мл, прибавляют 80 мл спирта (70 %, об/об) Р, обрабатывают ультразвуком в течение 15 мин и доводят до объема 100,0 мл этим же растворителем. Перемешивают и выдерживают в течение нескольких минут до оседания частиц.
Раствор сравнения. 10,0 мг ФСО хлорогеновой кислоты и 10,0 мг кофейной кислоты Р растворяют в спирте (70 %, об/об) Р, обрабатывают ультразвуком в течение 15 мин и доводят до объема 10,0 мл этим же растворителем. 4,0 мл полученного раствора разводят спиртом (70%, об/об) Р до объема 100,0 мл.
Условия хроматографирования:
- колонка длиной 0,25 м и внутренним диаметром 4,6 мм, заполненная силикагелем октадецилсилильным для хроматографии Р с раз-мером частиц 5 мкм;
- температура: 35°С;
- подвижная фаза:
- подвижная фаза А: кислота фосфорная Р — вода Р (1:999, об/об);
- подвижная фаза В: ацетонитрил Р;
- скорость подвижной фазы: 1,5 мл/мин;
- спектрофотометрический детектор, длина волны 330 нм;
- объем вводимой пробы: 10 мкл.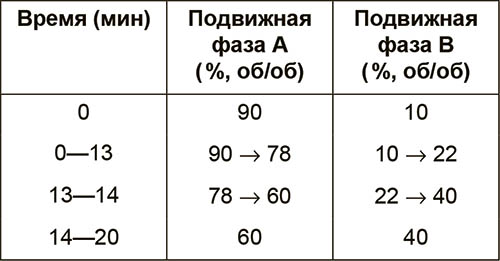
Относительные времена удерживания (по отношению к хлорогеновой кислоте, время удерживания около 7 мин): кафтаровая кислота — около 0,8; кофейная кислота — около 1,5; цинарин — около 1,6; эхинакозид — около 1,7; цикориевая кислота — около 2,3.
Пригодность хроматографической системы: раствор сравнения:
- разрешение между пиками кофейной кислоты и хлорогеновой кислоты не менее 5.
На хроматограмме раствора сравнения отмечают пики кофейной кислоты и хлорогеновой кислоты. На хроматограмме испытуемого раствора отмечают пики кафтаровой кислоты и цикориевой кислоты, используя хроматограмму на рисунке 1.
Содержание кафтаровой кислоты в процентах рассчитывают по формуле:
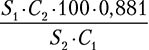
Содержание цикориевой кислоты в процентах рассчитывают по формуле: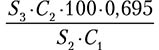
где:
S1 — площадь пика кафтаровой кислоты на хроматограмме испытуемого раствора;
S2 — площадь пика хлорогеновой кислоты на хроматограмме раствора сравнения;
S3 — площадь пика цикориевой кислоты на хроматограмме раствора сравнения;
С1 — концентрация испытуемого раствора, мг/мл;
С2 — концентрация хлорогеновой кислоты в растворе сравнения;
0,695 — коэффициент пересчета, учитывающий разную чувствительность детектора;
0,881 — коэффициент пересчета между кафтаровой кислотой и хлорогеновой кислотой.
Определение содержания суммы производных оксикоричных кислот в пересчете на цикориевую кислоту. 1,000 г измельченного сырья (500) помещают в колбу со шлифом вместимостью 25 мл, прибавляют 0,1 г кислоты щавелевой Р, вносят магнитный стержень с полимерным покрытием и прибавляют 10,0 мл спирта (95%, об/об) Р. Колбу с содержимым закрывают пробкой и взвешивают с точностью до 0,01 г. Нагревают с обратным холодильником при слабом кипении в течение 45 мин при постоянном перемешивании. Охлаждают, закрывают пробкой, взвешивают и, при необходимости, доводят спиртом (95 %, об/об) Р до первоначальной массы и перемешивают. Содержимое колбы центрифугируют при 3000 об/мин в течение 3 мин. Собирают надосадочную жидкость.
На линию старта листа фильтровальной бумаги размером 15x15 см наносят двумя полосами длиной 3 см по 20 мкл полученного раствора. После высыхания пятен отмечают их границы графитовым карандашом и хроматографируют восходящим способом (2.2.26), в качестве подвижной фазы используют хлороформ Р. Когда фронт подвижной фазы пройдет 5 см от линии старта, бумагу вынимают из камеры и высушивают на воздухе до удаления запаха хлороформа. Отмеченные участки стартовых пятен вырезают, помещают в колбы вместимостью 25 мл, приливают в каждую по 10,0 мл 0,1 М раствора кислоты хлористоводородной и встряхивают в течение 30 мин.
Измеряют оптическую плотность (2.2.25) полученных растворов при 328 нм, используя 0,1 М раствор кислоты хлористоводородной в качестве компенсационного раствора. Используют среднее значение оптической плотности полученных растворов.
Содержание суммы производных оксикоричных кислот в пересчете на цикориевую кислоту в процентах рассчитывают по формуле:
![]()
где:
782 — удельный показатель поглощения цикориевой кислоты;
А — среднее значение оптической плотности;
m — масса навески испытуемого сырья, г.
ХРАНЕНИЕ
В защищенном от влаги и света месте при температуре от 15°С до 25°С.